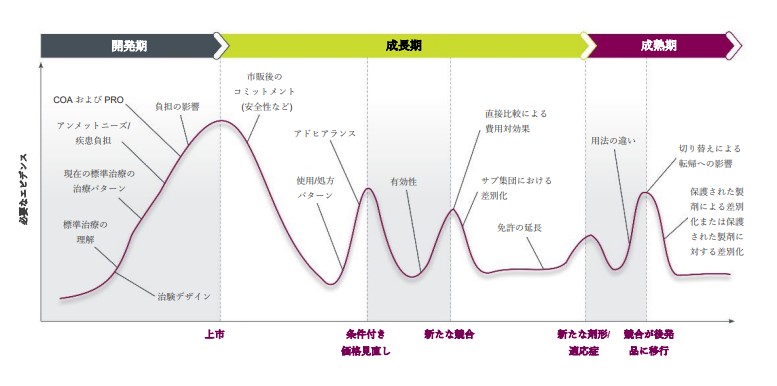
1. 開発期:臨床転帰評価の検証
神経学や精神医学領域の治験では、評価項目の選択と解釈が、主観性、自己申告、不均一性、プラセボ効果、意義、感度、併存疾患、評価者間のばらつきなどの要因により、依然として大きな課題となっています。新製品の価値を確立するには、臨床転帰評価 (COA) などの、正確で感度の高い、検証されたリアルワードの評価項目が必要です。これをRCTに組み込むと、疾患の重症度と疾患進行を、患者および適応症に関連して総合的に評価することができます。規制当局はCOAを主要及び副次的有効性評価項目として承認しており、保険者は定期的にCOAを精査して費用対効果とリアルワールドの結果を評価しています。
最適なCOAを選択によって (その後、規制当局と保険者にとって十分な厳密さでデータ収集・分析) アンメットニーズを実証することができます。たとえば、失調症の認知症状は、仕事、自立した生活、人間関係構築能力に悪影響を及ぼすことが多くなります。しかし、特に認知症状を緩和することで患者さんの生活の質 (QoL) を向上させる、承認済みの統合失調症治療はありません。
COAの構成 (理論的なフレームワーク) と内容 (具体的な質問、項目、またはタスク) を検証することが重要です。パレクセルは最近、患者さん、介護者、または医師のインタビューに基づいたCOAである、統合失調症認知評価尺度 (SCoRS) に対する介護者からのインプットを治験依頼者が検証できるよう支援しています。私たちは定性的な非介入試験をデザインし、有償で従事する専門の介護者と共に、この尺度の内容と明確さを確認しました 3。ほとんどの介護者が、この尺度の質問、項目、回答オプションを正確に解釈したことから、統合失調症に関連する認知問題の影響を介護者が評価できることが示唆されました。
パレクセルは別の治験依頼者と協力して、まれな神経変性障害である脊髄小脳失調症 (SCA) 患者さんのフリードライヒ運動失調症評価尺度における日常生活動作 (FARS-ADL) の関連性、明確性、および臨床的意義を評価しました。SCAでは小児が発達において重要なマイルストーンを逸すという重大なリスクにさらされ、思春期にあっても自己評価を実施できないため、特有の課題があります。医療従事者 (HCP) にとって尺度の明確さと使いやすさ、臨床的意義のある変化を捉える能力を検証することを目標としました。HCPによる判断では、FARS-ADL合計スコアの1~2点の増加で、臨床的意義のある進行を示すこと、任意の項目または合計スコアの1年以上の安定で疾患停滞とみなしていることを突き止めました 4。この治験依頼者は、第III相ピボタル試験の副次的評価項目としてFARS-ADLを使用し、最近新薬申請を提出しました。FDAはこれを承認し、優先審査を適用しています。
2. 開発期:対象患者集団の特定と登録
リアルワールドデータ (RWD) は対象患者集団を特定するために不可欠なもので、これによって代表的なサンプルを対象に新規治療の試験を実施できるようになります。病態の診断と治療が人種、民族、性別、地理、社会経済的地位によって大きく異なる場合、治験責任医師はRCTでの過少表現または過大表現のリスクを軽減する方法を理解する必要があります。それ以外の場合、HTA機関と保険者は償還を却下することができます。
片頭痛の治験への代表的な患者登録を加速するために、弊社はある治験依頼者と連携しています。世界保健機関は質の高い教育と医療へのアクセス、経済の安定性、社会およびコミュニティの背景、現地の環境など、医療以外の健康の社会的決定要因 (SDOH) が、健康転帰の30~55%を占めると推定しています 5。私たちは診断と治療によって3つの患者コホートを特徴付け、請求データを用いて、教育、収入、婚姻ステータス、SDOHで層別化しました。弊社は患者さんのニーズと医療従事者のパターンを分析することが、片頭痛患者さんをより代表する集団の特定と募集に役立つことを確認しました。またRWDにより、鍼灸師などの医療従事者や、代替医療施術者を特定することも可能です。
パレクセルでは健常ボランティアよりも、パーキンソン病 (PD) 患者を対象に早期治験の実施を検討している治験依頼者が増えています。しかし、PD患者は治療を意図しない投与を1回だけ受けることになるか、投薬を数回しか受けられないことがわかっているため、PD患者を第I相投与試験に参加させるのが難しいことがよくあります。さらにクリニックに1泊し、採血や腰椎穿刺を繰り返すなどの侵襲性手技を受けなければならないこともあります。弊社は米国の包括的な請求データソースから取得したRWDを活用し、PD患者を治療する運動障がいの専門家を対象に絞りました。その後、登録例数を増やすため、退職者の大規模なコミュニティの近郊にあるコミュニティに根付いた施設を対象にして、彼らをネットワークに登録。第I相試験では、この機会にしか受けられないであろう専門家からの特別なケアに前向きな退職患者を特定し、侵襲性手技に対して補償を行うことで募集を促進します。
3. 開発期および成長期:信頼性が高く、患者さんに優しいデジタル技術の選択
ウェアラブル機器や接続機器など、受動的にデータを収集するデジタル技術を用いることで、患者さんの負担が軽減され、募集と参加継続が促されます。ただし、これらの機器は感度と信頼性、患者さんにとっての使いやすさ、リアルタイムデータの収集機能、意義のある指標を評価できることを検証する必要があります。これはRCTや観察研究として重要な点です。
パーキンソン病などの神経変性疾患のある患者さんは、自身の障がいに対処することに追われています。新しいユーザーインターフェイスを習得したり、機器の充電や同期が欠かせないなど、患者さんは負担が増えることを望みません。
パレクセルでは、300件の分散型試験において140台以上の接続機器を検討しました。たとえば評価項目であるStride Velocity 95th Centile (SV95C) を用いて (マジックテープで足首に小型機器を装着して歩行速度を測定する)、デュシェンヌ型筋ジストロフィー (DMD) 試験を実施しました。機器を充電している夜間にデータが中央データベースに送信されます。ウェアラブル機器は日々の動作を一定期間記録するため、そのデータは、来院時の患者さんの意欲や疲れの程度に影響されません。2023年、EMAは診療所で実施する6分間の歩行テストに代わる、DMD試験の主要評価項目としてSV95Cを承認しました 6。米国ではFDAが副次的評価項目として、SV95Cを承認しています
パレクセルは最近、国内のある慈善団体と協力しながら、神経変性疾患の縦断的観察研究のためのデジタル機器と評価項目を選定する機会がありました。試験デザイン担当者は、活動トラッカーと脳波 (EEG) ヘッドセットを使用して、疾患の早期徴候を検出し、進行を追跡したいという考えでした。弊社からの推奨事項としては、将来得られる結果を守るために臨床的に検証された医療グレードの機器を利用すること、コンプライアンスを確保し受動的なデータ収集を合理化するために患者さんのトレーニングを行うこと、後に利用可能となり得るアルゴリズム、集計手法、統計分析を活用できるように、できる限り多くの生データを収集して保存することなどが挙げられます。
4. 成長期:承認後の安全性、有効性、使用の確立
治験依頼者は医薬品の使用パターンの調査、市販後の要件を満たすためにRWDを使用し、承認後の安全性と有効性に関する試験を実施します。承認後のリアルワールド試験では、運用に関する専門知識、規制上の期待値や業界標準への精通、科学的厳密さ、複雑なデータ処理と分析が求められます。
弊社では最近、慢性神経疾患における薬剤の長期使用と安全性を評価するために必須となる観察コホート試験をデザインして実施しました。RWDプラットフォームを活用し、3つのソースから100のデータセットの統合と集計を行っています。規制当局が8年間の年次報告書を要求したため、効率的で繰り返しが可能なデータ処理手順を策定しました。テクノロジーを基盤とするクエリ管理ソリューションを使用してデータをクリーニングし、ソース間の矛盾や競合を解決することで、データ品質を向上させています。
5. 成長期と成熟期:経済的価値の定量化と差別化
RWEは新規製剤や投与レジメンに対する服薬遵守など、RCTでは通常入手できないデータを収集することで、製品を差別化することができます。RCTではプロトコルで規定された治療スケジュールに厳密に従いますが、治験外で患者さんが薬を指示どおりに服用しない可能性があり、結果への悪影響が考えられます。リアルワールド試験では、そのような差異を捕捉することができます。
同様にRWDは、ある治療から別の治療への切り替えコストを定量化することができます。たとえばMS患者が治療を変更すると、多くの場合、脳MRIスキャン、診療所、看護師、救急治療室への来院、入院の利用増加が生じます。持続的な有効性と優れた忍容性を備えた製品は、競合他社よりも高い費用対効果を示すことがありますが、切り替えコストは十分に解明されていません。パレクセルはMS化合物の治験依頼者がオープンな請求リポジトリと電子健康記録 (EHR) からデータを収集して分析し、競争の激しい市場での切り替えのパターンと費用の特定、製品の差別化を支援しています。
新規治療の価値を定量化するには、疾患に固有の堅実な経済モデルが必要です。このモデルは疾患の経過と、患者さんの生活の質(QoL)および生産性への影響を保険者にとって理解しやすい指標で示す必要があります。しかし、多くの経済モデルが不完全であったり、時代遅れなものになっています。
パレクセルでは疾患に固有のモデルを継続的に分析し、科学的、技術的、臨床的進歩を取り入れるようにしています。たとえば最近ではMSモデル163例について、その進行、限界、構造を分析したところ、MRI (磁気共鳴画像) データを含むものは10%未満であることがわかりました 7。それでもT2病変やガドリニウム増強病変、脳容積減少の定量化など、MRIの技術的進歩により、長期的な疾患活動性や疾患進行の予測値が得られ、より正確な経済モデリングが可能になる場合があります 8。また、「最も信頼できる基準」となるMSモデルでは、再発と寛解のサイクルにおける疲労、労働生産性、または医療資源の利用は考慮されていません。弊社の結論としてはMSの複雑さを把握し、その経済的影響についてより良いインサイトを得られる、さらに洗練したモデリングの緊急の必要性と機会の局面を迎えていると捉えています。
商業的な実現可能性の持続にはRWEが不可欠
医薬品開発者は神経科学療法のライフサイクル全体を通して、RWEが価値提案の構成に欠くことができない要素であることを前提とすべきです。規制当局、HTA機関、保険者、および処方者は、全員が新製品の推奨、支払い、または処方に同意する前に新製品の利点とリスクについて、エビデンスに基づくプロファイルが必要であると考えています。
統合されたエビデンスを創出する計画は、成功するための最も確実なルートとなります。この計画によって多様なステークホルダーのニーズへの対応、RWEの影響の最大化や冗長性の削減が図られ、データ収集に適したテクノロジーを確実に選択できるためです。RWEの創出は長期的な取り組みです。早期に動き出せるかで、何年もの後の上市の成功が決まることがあります。
この記事の執筆にご協力いただいた皆様に感謝申し上げます。
Stacy Charlerie – Director, RWD Strategy, Real World Research
Karina D’Angelo – Director, RWD Strategy, Real World Research
Eliza Galvez – Senior Director, Integrated Solutions Strategy
Katja Hakkarainen – Vice President, Head of Epidemiology, Real World Research
Nathan Noakes – Director, Sensor Solutions, Real World Research
Jaime Roberts – Associate Director, Feasibility and Strategy
Jaime Smith – Senior Director, Head of RWD Strategy, Real World Research
Contributing Expert